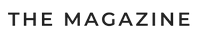Enerji kaynaklarının fiyatındaki artış, hanehalkı düzeyi de dahil olmak üzere daha verimli ve daha ucuz yakıt türlerinin araştırılmasını teşvik eder. Çoğu hevesli zanaatkar, kalorifik değeri metandan üç kat daha fazla olan hidrojenden etkilenir (38.8 kW ve 1 kg madde ile 13.8). Evde ekstraksiyon yöntemi, görünüşe göre, bilinen - suyun elektroliz ile bölünmesi. Aslında, sorun çok daha karmaşıktır. Yazımızın 2 hedefi var:
- bir hidrojen jeneratörünün minimum maliyetle nasıl yapılacağı sorusunu analiz etmek;
- özel bir evi ısıtmak, araba doldurmak ve kaynak makinesi olarak hidrojen jeneratörü kullanmayı düşünün.
Kısa teorik bölüm
Hidrojen, yani hidrojen, - periyodik tablonun ilk elemanı - yüksek kimyasal aktiviteye sahip en hafif gazlı maddedir. Oksidasyon sırasında (yani yanma), sıradan su oluşturan büyük miktarda ısı yayar. Elemanın özelliklerini karakterize ederek onları karakterize ediyoruz:
- Hidrojen yanması çevre dostu bir işlemdir, zararlı madde salmaz.

- Kimyasal aktivitesi nedeniyle dünyada serbest gaz oluşmaz. Ancak suyun bileşiminde rezervleri tükenmez.
- Element endüstriyel üretimde, örneğin kömürün gazlaştırılması (piroliz) işleminde kimyasal bir yöntemle ekstrakte edilir. Genellikle bir yan ürün.
- Gazlı hidrojen elde etmenin bir başka yolu, katalizörler - platin ve diğer pahalı alaşımlar varlığında suyun elektrolizidir.
- Basit bir hidrojen + oksijen (oksijen) gaz karışımı en ufak bir kıvılcımdan patlayarak anında büyük miktarda enerji açığa çıkarır.
Referans için. Su molekülünü önce hidrojen ve oksijene ayıran bilim adamları, patlama eğilimi nedeniyle karışımı patlayıcı gaz olarak adlandırdılar. Daha sonra Brown'un gazını (mucit adına) aldı ve STK'ların varsayımsal formülü ile belirlendi.

Yukarıdakilerden, aşağıdaki sonuç kendini göstermektedir: 2 hidrojen atomu, 1 oksijen atomu ile kolayca birleşir, ancak ayrılmak istemezler. Kimyasal oksidasyon reaksiyonu, aşağıdaki formüle uygun olarak termal enerjinin doğrudan salınımı ile devam eder:
2H2 + O2 → 2H2O + Q (enerji)
İşte uçuşların daha ayrıntılı analizinde bizim için yararlı olacak önemli bir nokta yatıyor: hidrojen ateşlemeden kendiliğinden reaksiyona giriyor ve ısı doğrudan açığa çıkıyor. Bir su molekülünü ayırmak için enerjinin harcanması gerekecektir:
2H2O → 2H2 + O2 - S
Bu, elektriği sağlayarak suyun ayrılması işlemini karakterize eden bir elektrolitik reaksiyon formülüdür. Bunu nasıl uygulayacağınız ve kendi ellerinizle bir hidrojen jeneratörü nasıl yapacağınız, daha fazla düşüneceğiz.
Prototip oluşturma
Ne ile uğraştığınızı anlamanız için, önce en basit hidrojen jeneratörünü en düşük maliyetle monte etmenizi öneririz. Ev yapımı bir kurulumun tasarımı şemada gösterilmiştir.

İlkel bir elektrolizör aşağıdakilerden oluşur:
- reaktör - kalın duvarlı cam veya plastik kap;
- bir reaktöre su ile daldırılmış ve bir güç kaynağına bağlanmış metal elektrotlar;
- ikinci tank bir su kapağı görevi görür;
- HHO gaz egzoz boruları.
Önemli bir nokta. Elektrolitik hidrojen ünitesi sadece doğru akımdan çalışır. Bu nedenle, güç kaynağı olarak AC adaptörünü, araç şarj cihazını veya pili kullanın. Bir alternatör çalışmaz.
Elektrolizörün çalışma prensibi aşağıdaki gibidir:
- Suya batırılmış iki elektrot, tercihen ayarlanabilir bir kaynaktan voltaj ile beslenir.Reaksiyonu iyileştirmek için, kaba (evde - normal tuz) biraz alkali veya asit eklenir.
- Elektroliz reaksiyonunun bir sonucu olarak hidrojen, “eksi” terminaline bağlı katodun yanından serbest bırakılacak ve anodun yakınında oksijen üretilecektir.
- Karıştırma, her iki gazın da bir tüp vasıtasıyla 2 işlevi yerine getiren bir su tuzağına girer: su buharının ayrılması ve reaktördeki bir flaşın önlenmesi.
- İkinci tanktan, NNO'nun patlayıcı gazı, su oluşturmak için yakıldığı brülöre beslenir.
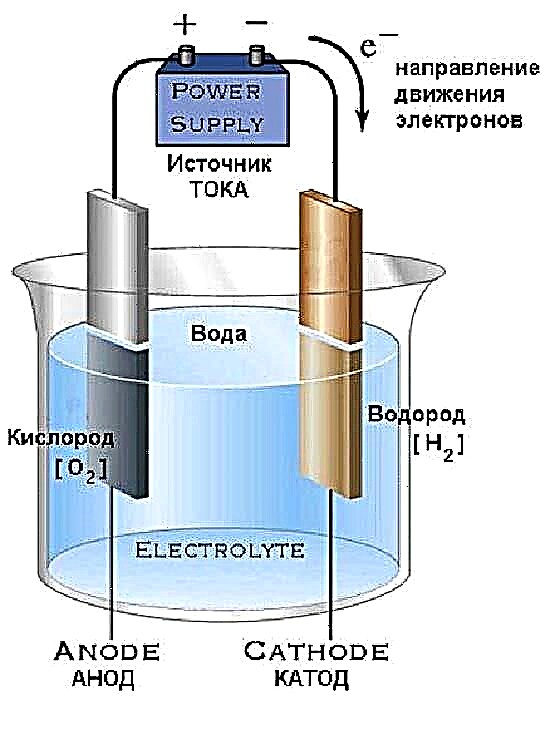
Şemada gösterilen jeneratör tasarımını kendi ellerinizle yapmak için geniş boyunlu ve kapaklı 2 cam şişeye, tıbbi bir damlalığa ve 2 düzine vidaya ihtiyacınız olacak. Fotoğrafta tam bir malzeme seti gösterilmektedir.

Özel aletlerden plastik kapakları kapatmak için bir tutkal tabancası gereklidir. Üretim prosedürü basittir:
- Düz tahta çubukları, uçlarını farklı yönlere yerleştirerek vidalarla bükün. Vida kafalarını birbirine lehimleyin ve kabloları bağlayın - gelecekteki elektrotları alın.
- Kapakta bir delik açın, damlalık ve kabloların kesilmiş kasasını oraya yerleştirin, ardından her iki taraftan bir tutkal tabancasıyla kapatın.
- Elektrotları şişeye yerleştirin ve kapağı vidalayın.
- İkinci kapakta 2 delik açın, damlalık tüplerini takın ve düz su ile doldurulmuş bir şişeye vidalayın.
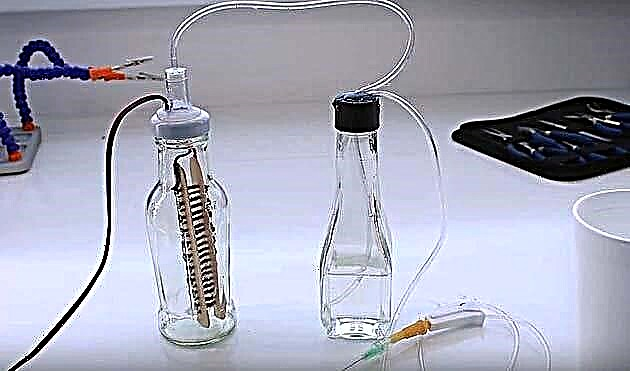
Hidrojen jeneratörünü başlatmak için, tuzlu suyu reaktöre dökün ve güç kaynağını açın. Reaksiyonun başlangıcı, her iki kaptaki gaz kabarcıklarının ortaya çıkması ile işaretlenir. Gerilimi optimum değere ayarlayın ve damlalık iğnesinden çıkan Kahverengi gaza ateşe verin.
Meyer hidrojen hücresi hakkında
Yukarıda açıklanan tasarımı yaptıysanız ve test ettiyseniz, iğnenin ucundaki alevi yakarak kurulum performansının son derece düşük olduğunu fark etmişsinizdir. Daha fazla patlayıcı gaz elde etmek için, mucit onuruna Stanley Meyer hücresi olarak adlandırılan daha ciddi bir cihaz yapmanız gerekir.
Hücrenin çalışma prensibi ayrıca elektrolize dayanır, sadece anot ve katot, birbirine sokulan tüpler şeklinde yapılır. Voltaj puls üretecinden, akım tüketimini azaltmaya ve hidrojen jeneratörünün verimliliğini artırmaya izin veren iki rezonant bobin yoluyla sağlanır. Cihazın elektronik devresi şekilde gösterilmiştir:

Not. Şemanın çalışmasıyla ilgili ayrıntılar http://www.meanders.ru/meiers8.shtml kaynağında açıklanmaktadır.
Meyer hücresi yapmak için ihtiyacınız olacak:
- plastik veya pleksiglastan yapılmış silindirik bir kasa; ustalar genellikle kapaklı ve nozullu bir su filtresi kullanır;
- 15 ve 20 mm çapında, uzunluğu 97 mm olan paslanmaz çelik borular;
- teller, izolatörler.

Korozyona dayanıklı borular dielektrik tabanına tutturulur, jeneratöre bağlı teller lehimlenir. Hücre, fotoğrafta gösterildiği gibi plastik veya pleksiglas bir kutuya yerleştirilmiş 9 veya 11 tüpten oluşur.

Elemanlar, bir elektronik ünite, bir Meyer hücresi ve bir su kilidi (teknik adı fıskiye) içeren İnternet'te bilinen tüm şemalara göre bağlanır. Güvenlik nedeniyle, sistem kritik basınç ve su seviyesi sensörleri ile donatılmıştır. Ev ustalarının incelemelerine göre, böyle bir hidrojen tesisatı, 12 V'luk bir voltajda 1 amperlik bir akım tüketir ve kesin sayılar mevcut olmamasına rağmen yeterli performansa sahiptir.

Plaka Reaktörü
Bir gaz brülörünün çalışmasını sağlayabilen yüksek performanslı bir hidrojen jeneratörü, 15 x 10 cm boyutlarında paslanmaz plakalardan yapılmıştır, sayı 30 ila 70 adettir. Çıtçıtları sıkmak için delikler delinir ve teli bağlamak için bir terminal köşede kesilir.

316 kalite saclara ek olarak, şunları satın almanız gerekecektir:
- Alkaliye dayanıklı 4 mm kalınlığında kauçuk;
- pleksiglas veya textolitten yapılmış uç plakaları;
- bağlantı çubukları M10-14;
- gaz kaynağı aparatı için çek valf;
- bir hidrolock altında su filtresi;
- oluklu paslanmaz çelikten bağlantı boruları;
- toz halinde potasyum hidroksit.

Plakalar, çizimde gösterildiği gibi, orta kesikli kauçuk contalarla izole edilmiş tek bir üniteye monte edilmelidir. Elde edilen reaktörü çıtçıtlarla sıkıca çekin ve elektrolit nozullarına bağlayın. İkincisi, bir kapak ve kapatma valfleri ile donatılmış ayrı bir kaptan gelir.
Not. Bir akış (kuru) tipi elektrolizörün nasıl yapılacağını söyleriz. Daldırma plakaları olan bir reaktör yapmak daha kolaydır - kauçuk contalara gerek yoktur ve monte edilen ünite elektrolitli kapalı bir kaba indirilir.

Hidrojen üreten bir jeneratörün müteakip montajı aynı şekilde, ancak farklılıklar ile gerçekleştirilir:
- Cihazın kasasına elektrolitin hazırlanması için bir tank eklenmiştir. İkincisi, su içinde% 7-15'lik bir potasyum hidroksit çözeltisidir.
- Su yerine, deoksidizatör - aseton veya inorganik bir çözücü - “fıskiye” içine dökülür.
- Brülörün önüne bir çek valf yerleştirilmelidir, aksi takdirde hidrojen brülörü sorunsuz bir şekilde kapatıldığında hortumları ve fıskiyeyi ters çevirir.
Evde hidrojen almak karlı mı?
Bu sorunun cevabı oksijen-hidrojen karışımının kapsamına bağlıdır. Çeşitli çevrimiçi kaynaklar tarafından yayınlanan tüm çizimler ve diyagramlar, aşağıdaki amaçlar için HHO gazı üretmek üzere tasarlanmıştır:
- arabalar için yakıt olarak hidrojen kullanın;
- ısıtma kazanlarında ve sobalarda dumansız olarak hidrojen yakmak;
- gaz kaynağı için uygulayın.
Hidrojen yakıtının tüm avantajlarını aşan ana sorun: saf maddenin salınımı için elektrik maliyeti, yanmasından alınan enerji miktarını aşmaktadır. Ütopik teorilerin taraftarları ne olursa olsun, elektrolizörün maksimum verimliliği% 50'ye ulaşır. Yani 1 kW ısı 2 kW elektrik tüketir. Fayda sıfır, hatta negatif.
 İlk bölümde yazdığımızı hatırlayın. Hidrojen çok aktif bir elementtir ve kendi başına oksijen ile reaksiyona girerek çok fazla ısı üretir. Kararlı bir su molekülünü ayırmaya çalışırken, enerjiyi doğrudan atomlara getiremeyiz. Yarma elektriği, suyu, trafo sargılarını vb. Isıtmak suretiyle dağıtılan elektrikle gerçekleştirilir.
İlk bölümde yazdığımızı hatırlayın. Hidrojen çok aktif bir elementtir ve kendi başına oksijen ile reaksiyona girerek çok fazla ısı üretir. Kararlı bir su molekülünü ayırmaya çalışırken, enerjiyi doğrudan atomlara getiremeyiz. Yarma elektriği, suyu, trafo sargılarını vb. Isıtmak suretiyle dağıtılan elektrikle gerçekleştirilir.
Önemli arka plan bilgileri. Hidrojen yanmasının özgül ısısı metan sıcaklığından üç kat daha yüksektir, fakat kütlece. Bunları hacme göre karşılaştırırsak, 1 m³ hidrojen yakarken, metan için 11 kW'a kıyasla sadece 3,6 kW termal enerji açığa çıkacaktır. Sonuçta, hidrojen en hafif kimyasal elementtir.
Şimdi, ev yapımı bir hidrojen jeneratöründe elektrolizle elde edilen patlayıcı gazı yukarıdaki ihtiyaçlar için yakıt olarak düşünün:
- Son kurulum fiyatı, düşük verimlilik ve verimlilik, özel bir evi ısıtmak için hidrojen yakmayı son derece kârsız hale getirir. TEN, indüksiyon veya elektrot gibi herhangi bir elektrikli kazanı, sayacı bir elektrolizörle "sarmak "tan daha kolaydır.
- Bir araba için 1 litre benzin değiştirmek için, üçte biri oksijen olan 4.766 litre saf hidrojen veya 7.150 litre patlayıcı gaz gerekecektir. İnternetteki en berbat mucit henüz benzer performans sağlayabilen bir elektrolizör üretmedi.

- Hidrojeni yakan bir gaz kaynak cihazı, asetilen, propan ve oksijen içeren silindirlerden daha kompakt ve daha hafiftir. Ayrıca, 3000 ° C'ye kadar alev sıcaklığı herhangi bir metalle çalışmanıza izin verir, burada yakıt elde etme maliyeti özel bir rol oynamaz.
Referans için. Bir kazanda hidrojeni yakmak için, bir hidrojen brülörü herhangi bir çeliği eritebileceğinden yapıyı iyice yeniden tasarlamak zorunda kalacaksınız.
Sonuç
Ev yapımı bir hidrojen üreticisinden elde edilen STK gazının bileşimindeki hidrojen iki amaç için yararlıdır: deneyler ve gaz kaynağı.Elektrolizörün düşük verimliliğini ve tüketilen elektrikle bir araya getirmenin maliyetlerini atlasak bile, binayı ısıtmak için yeterli verimlilik yoktur. Bu aynı zamanda binek otomobilin benzinli motoru için de geçerlidir.